近日,基础医学院病理教研室/第一附属医院病理科吴正升教授团队联合浙江大学等单位在国际期刊《研究(Research)》(中科院一区Top,IF=10.9)在线发表题为《ARTS通过Livin-MDM2-p53信号通路诱导凋亡依赖的自噬促进乳腺癌化疗耐药(ARTS Confers ChemoresistanceofBreast Cancer by Inducing Apoptosis-Dependent Autophagy via Livin-MDM2-p53 Pathway)》的研究论文。我校教授吴正升、高级实验师王晓楠和浙江大学第一附属医院研究员黄星为本文通讯作者,基础医学院副教授丁克硕、博士研究生王浩、沈玉婷、第一附属医院郭欠影和浙江大学硕士研究生陈崟峰为论文共同第一作者。我校为论文第一单位。
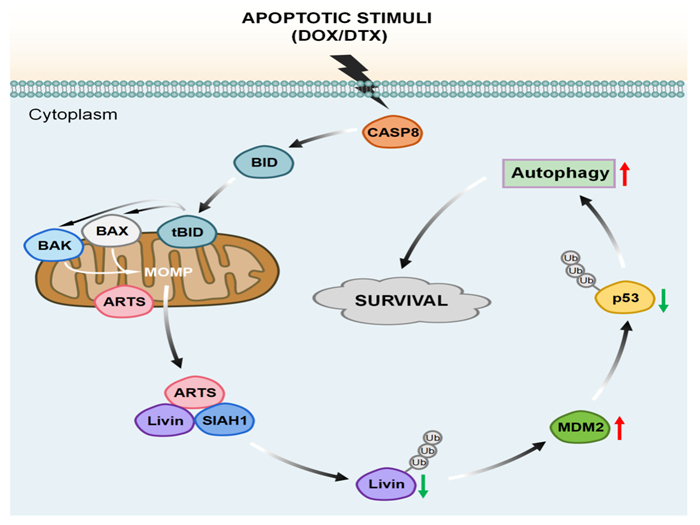
化疗是乳腺癌治疗的重要手段,但肿瘤细胞耐药会导致治疗失败。该研究聚焦“凋亡-自噬”互作在耐药中的作用,提出并验证了一个关键分子枢纽:转化生长因子(TGF-B)信号通路相关的凋亡相关蛋白(ARTS)可将凋亡信号“转接”到自噬,从而促使肿瘤细胞在化疗压力下存活并获得耐药性。研究团队在新辅助化疗乳腺癌组织中结合转录组筛选与临床队列验证发现:在耐药肿瘤组织中ARTS表达水平更高,且与较差的临床病理特征、较高增殖指数和不良预后相关。在功能与机制层面,研究表明ARTS可通过诱导“保护性自噬”增强乳腺癌细胞对阿霉素和多西他赛的耐受;在化疗诱导的促凋亡信号下,ARTS从线粒体外膜转位至胞质,并通过触发缺失七同源蛋白1(SIAH1)介导的含杆状病毒IAP重复序列蛋白7(Livin)降解,继而激活小鼠双微体2同源蛋白(MDM2)-肿瘤蛋白p53(p53)轴,最终促进自噬并推动细胞存活。进一步实验还显示,抑制半胱天冬酶或阻断自噬通量可削弱ARTS介导的耐药表型,提示该通路具有潜在干预价值。
该成果首次提出“ARTS-Livin-MDM2-p53”作为连接凋亡与自噬的关键通路在乳腺癌化疗耐药中的发挥了重要作用。这一发现为理解乳腺癌获得性化疗耐药提供了新的机制框架,并为化疗联合靶向自噬/凋亡相关节点以克服耐药提供了新的理论依据和实验基础。
本研究获国家自然科学基金 (82473059,31970696,82103572)、安徽省自然科学基金(2408085MH218)和KY.COM开云体育(中国)科技公司科研水平提升计划(2021xkjT005)等项目支持。(基础医学院 学科科研办公室)
论文链接:https://spj.science.org/doi/10.34133/research.1086


